画期的な手法で、より効果的な新型コロナウイルスワクチンの開発に一歩近づく

2020年、世界的に大流行し2百万人もの命を奪った新型コロナウイルス感染症の拡大を封じ込めようと、100社以上もの製薬会社が、安全で効果的なワクチンの開発に急遽取り組みました。現在、実際に投与や臨床試験が行われているワクチンのほとんどが、不活化ワクチンと呼ばれるものです。一方、ウイルス学を専門とする東京大学 生産技術研究所(以下、生研)の米田 美佐子 特任教授は、麻疹ウイルスをベクター(遺伝子を細胞に届けるツール)として用い、遺伝子組換え生ワクチンを開発するという独自のアプローチで開発に邁進しています。

米田特任教授は数年前、インドやバングラデシュで流行する動物由来感染症「ニパウイルス感染症」の対策に、麻疹ウイルスベクターを用いたワクチンを開発し、これが高い効果を発揮することを実感しました。この経験から、2020年に新型コロナウイルスの感染爆発を目の当たりした時、遺伝子組換えウイルスを使った同じ手法で生ワクチンを開発できると考えました。
米田特任教授ら研究チームは2020年9月、日本医療研究開発機構(AMED)の助成を受け、ワクチン製造に適した遺伝子組換えウイルスの実験をバイオセーフティレベル2のラボ(ウイルスなど微生物・病原体を扱う研究室)で開始しました。わずか1、2か月で、スパイク(S)タンパク質(新型コロナウィルス感染症の抗原で、ワクチンの標的)を発現させる遺伝子組換え麻疹ウイルスの合成に成功。ハムスターを使った実験では、この遺伝子組換えウイルスが新型コロナウイルス感染症の予防効果があると確認されています。実際のワクチン製造は近日中に始まる予定で、動物実験を2021年中に、第1相臨床試験を2022年初めに開始することを目標にしています。
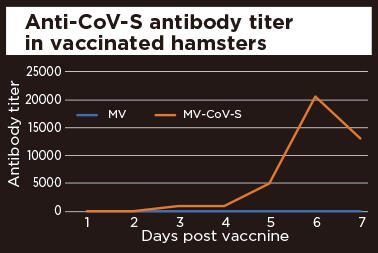
ワクチン接種したハムスターにおける抗コロナSタンパク抗体価の上昇
ハムスターに本研究チームが開発した新型コロナウイルスのSタンパクを発現する組換え麻疹ワクチン(MV-CoV-S)を2回接種したのち、血中抗コロナS抗体価の推移を示す。ワクチン接種したハムスターでは抗体価の著しい上昇が認められ、本ワクチンが新型コロナウイルスに対する免疫を誘導することが確認された。
米田特任教授は、「この生ワクチンで終生免疫が獲得できます。不活化ワクチンのように、半年や1年ごとに定期的にワクチンを接種する必要がありません」と、生ワクチンの有効性を強調します。
不活化ワクチンは、「抗原」(ウイルスが持つ特有のタンパク質)に反応して異物を排除する働きがある「抗体」だけを誘導するため、効果が弱く、一過性に過ぎないといいます。それに対し、生ワクチンは毒性を弱めた生ウイルスを使用するため、抗体だけではなく、「細胞性免疫」を誘導します。細胞性免疫とは、免疫を担当する細胞が、感染した細胞内の抗原を攻撃し、破壊する免疫反応です。
現在までに承認された、新型コロナウイルス感染症に対する唯一のウイルスベクターワクチンは、アデノウイルスをベクターとしたものですが、増殖欠損型ウイルスなので感染後生ワクチンのように体内で増えることができません。そうすると細胞性免疫も誘導はできるものの、効果はやや低く、免疫持続期間も長くはありません。米田特任教授は、つまり麻疹ウイルスを使ったものの方が効果は高いと指摘します。
生ワクチンの弱点を乗り越える
生ワクチンにも弱点があると指摘されています。生ウイルスを使用するため、体内でベクターと使用されたウイルスが強毒化する恐れがあるほか、ウイルスを無毒化した不活化ワクチンと比べ、安全性の確認試験に時間を要します。
しかし、米田特任教授は、「麻疹ワクチンとしては、1960年代から世界中で生ウイルスが使用されており、その安全性は確認されて久しい」と、安全性の問題はないとしています。ベクターは、抗原を細胞まで運び、その遺伝子コードを細胞内に侵入させる役割を果たします。事実、米田特任教授が開発に関わったニパウイルス感染症のワクチンは、その安全性が確認され、感染症流行対策イノベーション連合(CEPI:新興感染症のワクチン開発を促進する世界的な組織)との恊働で近く実用化される予定だといいます。
もう一つの課題は、遺伝子組換えでいかにSタンパク質をベクターに組み込むか、でした。
「近年まで、麻疹ウイルスのようなマイナス・一本鎖RNAウイルスの遺伝子組換えは難しいとされてきました」と米田特任教授が語るように、従来の方法では困難が伴いました。そこで使用したのが、ニパウイルス感染症ワクチン製造の際に開発した新技術でした。サポーティングプラスミド(染色体とは独立して複製を行う細胞内の遺伝子構造)を利用して感染性ウイルスを作成するもので、それによって遺伝子組換えが楽に行えるようになったそうです。
最後に残った高いハードル
新型コロナ感染症の生ワクチン開発で残る難題は、ワクチンの製造・販売を請け負う製薬会社を探し出すことです。
生ワクチンはその安全性を徹底的に検証しなければならないので、不活化ワクチンに比べて開発費が高くなります。また、生ワクチンで終生免疫を獲得できるので、ワクチンの製造数を大幅に抑えることができますが、製薬会社にとっては採算性がないということになります。
「このワクチンを世に出すには、ビル&メリンダ・ゲイツ財団のような慈善団体の協力が必要かもしれません」と米田特任教授。これまで複数の製薬会社とワクチンの製造・販売をめぐる協議を行なったものの不調に終わった、と明かしてくれました。
ワクチン接種による恩恵がリスクを上回るとして、米国などの諸国は、ファイザーやモデルナなどのワクチンの緊急使用を承認しています。米田特任教授は、同様に日本の医薬品の承認審査をする医薬品医療機器総合機構(PMDA)が早期にこのワクチンを承認することに期待感を示しています。PMDAとは、すでにワクチン製造およびその後の試験について相談しているといい、臨床試験完了後の速やかな承認を求めています。
研究結果で社会貢献を
米田特任教授がウイルス研究を始めたのは、東京大学 大学院農学生命科学研究科の博士課程に在籍していた時でした。ウイルスが特定の生物のみを宿主とする「宿主特異性」に興味を持ったといい、当初、ワクチンには目が行かなかったそうですが、ニパウイルスの研究をきっかけにワクチンの開発を開始しました。
その後、検査キット開発プロジェクトの一環でバングラデシュのニパウイルス感染症流行地域を訪れ、劣悪な衛生状態を目の当たりにしました。「開発したワクチンで貢献したい」と、ワクチン研究者としての意識が大きく変わったと言います。
新型コロナウイルスワクチンの開発でも、発展途上国の人々の衛生状況を大きく改善できると、米田特任教授は考えています。「社会貢献をできる大きなチャンス。技術や知見を積み上げて、社会的な問題の解決に寄与したい」と、今後の抱負を語ってくれました。
(記事執筆:(株)J-Proze 森 由美子)
関連記事
・英文広報誌「UTokyo-IIS Bulletin」Vol. 7を公開しました
